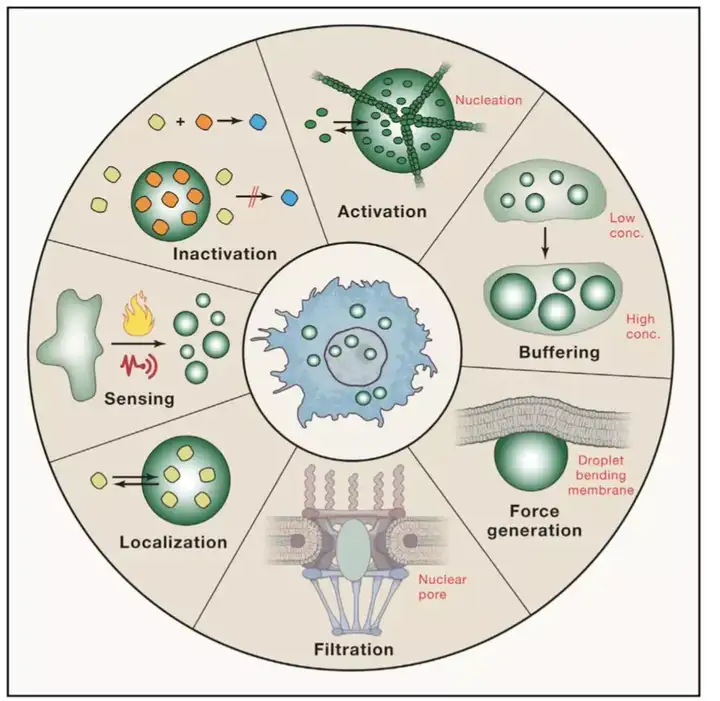
Germline P granules are liquid droplets that localize by controlled dissolution / condensation :细胞内通过“相分离”,可以提供一种特定的方式让细胞内的特定分子聚集起来,从而在“混乱的”细胞内部形成一定“秩序”,为困扰了大家多年的问题,提供了全新的思路。近几年的研究表明,**液-液相分离**(LLPS:liquid-liquid phase separation)可能是细胞形成无膜细胞器的物理化学基础,比如细胞内的p granule, nucleolar, stress granule等
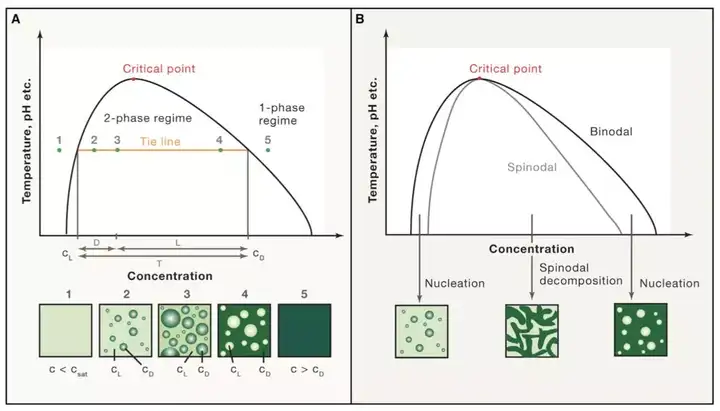
高度依赖溶液中生物大分子(比如:蛋白,DNA以及RNA等)的浓度、物理化学性质,以及溶液所处的环境,比如:温度、pH、盐离子浓度、盐离子类型以及溶液中存在其它的生物大分子。作者使用如下的Phase Diagram来描述这些与相分离相关的条件与该溶液是否发生相分离的关系。
图2:Schematic Phase Diagram

[ ] **相分离的形式:形成相分离后,该生物大分子有两种存在形式:在溶液中的低浓度状态,形成的“液滴”中较高浓度的形式**(另外,LLPS不仅能形成液滴状的结构,还能继续转变为**胶状物**的形式。**凝胶状态的相分离经常不可逆转**,这也为阿尔兹海默症等体内形成的amyloid-like fibers的形成,提供了全新的思路,为相关药物的设计提供了全新的理念。已有研究表明一些蛋白的突变会加快这种LLPS向凝胶状态转化的过程。)
随着相关条件的变化,两种形式可以相互转化- - - -相分离是一种高度动态的过程。
[ ] 相分离的预测:液-液相分离的发生是蛋白质和核酸在某种特定的情况下的一个普遍特性,然而多数相分离根本不可能发生在一个正常的细胞中。
<aside> 🍁 近几年涌现了许多对在生理状态下能够发生相分离的分子的普遍特征的研究:支架及客户蛋白的理论
支架分子被认为是相分离的驱动分子,而在相分离形成以后参与到液滴当中的则被称为是客户蛋白。支架蛋白与客户蛋白的相分离需要一个互作网络的形成,该网络常由蛋白质-蛋白质互作及蛋白质-RNA互作构成。
两种蛋白质类型参与促进此类互作网络的形成:
以多个折叠的结构域为特点**,如Nck蛋白中的SH3结构域,该结构域能够与短的线性模块如SLiMs相结合;以内部无序区(IDR)为特点**。两类蛋白有多处相似,其中最重要的一点是:蛋白间都通过多个结构域或模块相互作用。因此,通过从基因上初步推断蛋白的化合价可以判断该蛋白形成相分离的能力及饱和浓度。对RNA而言,特定的RNA可驱动相分离的发生,而一些含有IDR的蛋白包含多个RNA结合结构域、其目的RNA也包含多个蛋白结合序列。因此,蛋白和RNA能够通过多种方式形成多价互作,这些互作决定着特定蛋白及核酸形成相分离的能力。
</aside>
因此,目前常应用预测算法推测蛋白质中的IDR以分析其发生相分离的能力。
[ ] 体外重构相分离
相分离可以在体外通过纯化的蛋白以及核酸等在特定的条件下发生(2012年,美国西南医学中心Michael Rosen和Steven McKnight独立发现在试管中这些分子通过微弱的作用力形成液滴,即首次证实了相分离能够通过简单的生化实验在体外重复)。
体外相分离的体外实验存在一定的局限性。体外相分离实验最大的优势是在于其各个组分以及各个组分的浓度,以及各种外在条件(比如:温度,pH等条件)可以被严格控制,更加方便我们去研究相分离现象。因此,需要注意的是,相关的蛋白以及RNA、DNA等各个组分的纯度是至关重要的。在此,作者提出了用于体外相分离实验的蛋白以及核酸样品的表达纯化,保存以及样品处理的标准。
[ ] 相分离的物理特性
相分离液滴的物理状态变化极大。从液滴样直至多孔固体或胶体,其特性**取决于相分离中的分子构成、时间、液滴的稳定程度、淬灭深度等**。RNA的参与也可以影响相分离液滴的物理状态,但由于RNA既提供了多价结合位点、又贡献了静电,尚不清楚RNA究竟使其更流体化还是更固态化。由于不可逆的固态常被认为是一种病理状态,因此调控相分离的物理状态的因素仍有待进一步探究。
体外重现相分离时,有多种方法可对液滴的物理性质进行具体描述。
测量表征表面张力的反毛细管速度,辅以被动微流变学体外重现相分离现象时,对液滴物理特性的研究手段不胜枚举:如可利用延时显微镜测量液滴的反毛细管速度、通过FRAP测量液滴的流动性。然而如何探究体内相分离液滴的物理性质仍是一个难题。目前已有的手段如基因编码的纳米粒(GEMS)、荧光共振能量转移技术(FRET)、定量相显微镜(QPM)、折射率层析成像技术及更先进的布里渊显微镜等都可对体内相分离液滴的物理特性进行初步描绘。此外,体内相分离液滴的生物学功能也是研究的重点之一,如何改变液滴的性质以观察其功能,是未来的研究重点。
[ ] 检测细胞内的相分离现象
目前相分离领域的一个难点就是如何去鉴别细胞内的一些特殊的结构是否真的是相分离形成。在体外特定条件下,一些蛋白和RNA在足够的浓度或者合适的Buffer的情况下会发生相分离现象,通常通过在细胞内过表达这些蛋白,观察到形成较大的,球状的结构,以此来推测细胞内低浓度的该蛋白仍然会形成相分离,只是在普通的光学显微镜下无法检测到而已。然而,相分离需要足够浓度才能发生,因此,在使用过表达蛋白检测相分离的时候一定要考虑到外源过表达带来的影响。同时应该致力于寻找除过度表达之外的其他方式去证明细胞内确实发生了相分离现象。
溶液会从澄清变得浑浊,镜检时会看到在溶液中会存在一些如水中的油滴状态的液滴。应用高分子化学来指导相分离研究的可行性及局限性
液液相分离研究的目标之一,是建立能够解释和预测大分子相分离现象的理论体系,并通过一级序列预测相分离的饱和浓度、刺激因素、液滴状态。高分子化学中的弗洛里赫金斯理论描述的是由焓介导的均聚合物从贫溶剂中析出的化学基础,其扩展理论考虑到了这一过程中的静电力作用。无规相近似方法则仅仅考虑了带电氨基酸的序列特征对杂聚体的形成的影响。此外,通过近似模拟也可以对相分离现象的机制进行进一步发掘:对单分子蛋白的模拟已能够较准确的说明其序列和功能间的关系,然而对成百上千个分子构成的相分离现象的建模及分析仍是目前的难点之一。对多组分相分离系统的粗粒化模拟初步解释了多层无膜细胞器如核仁形成的物理机制:蛋白-蛋白间、蛋白-RNA间的相互作用由序列决定;而不同细胞组分之间的相互作用呈互斥或亲和的状态,则可最终导致非随机的多层结构的形成。
算法模拟及理论体系可作为相分离现象实验数据的有力补充。反之,体内相分离现象的实验描述可作为算法模拟的数据库、并从中产生能够描述多分子复杂相分离现象的新的理论。
相分离研究的重点还是在于对其生物学功能的阐述